在医疗器械行业快速发展的今天,合规性是确保产品成功上市并持续运营的关键。中国作为全球重要的医疗器械市场,其法规体系日益完善且要求严格,企业需应对从产品注册、生产质量管理到上市后监督的全周期监管。杭州瑞旭科技集团作为国内领先的技术咨询服务机构,专注于为中国及国际医疗器械企业提供全面、专业的法规咨询服务,助力企业高效应对合规挑战,加速市场准入。
一、中国医疗器械法规环境概述
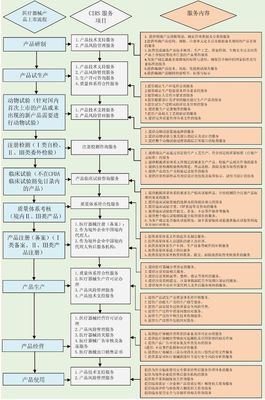
中国的医疗器械监管遵循《医疗器械监督管理条例》为核心的法律框架,由国家药品监督管理局(NMPA)负责实施。根据风险等级,医疗器械分为一类、二类和三类,监管要求逐级提高。企业需完成产品备案或注册、生产许可、临床试验(如适用)、质量体系核查等环节,流程复杂且耗时较长。NMPA持续推进法规与国际接轨,如加入国际医疗器械监管机构论坛(IMDRF),但本土化要求依然显著,企业常面临法规解读不清晰、申请材料准备繁琐等难题。
二、杭州瑞旭科技集团的核心服务领域
杭州瑞旭科技集团凭借多年行业经验,构建了覆盖医疗器械全生命周期的咨询服务体系,主要包括:
- 产品注册与备案支持:针对不同类别医疗器械,提供从分类界定、注册路径规划到申报资料编写的全程辅导。团队熟悉NMPA最新指南,能帮助企业优化技术文件,提高注册成功率。例如,对于创新医疗器械,瑞旭可协助申请绿色通道,缩短审批时间。
- 质量管理体系合规:依据《医疗器械生产质量管理规范》(GMP)要求,为企业建立或优化质量体系,包括文件管理、生产过程控制、供应商审核等。瑞旭提供培训和现场指导,确保企业通过NMPA的体系核查,并持续符合ISO 13485等国际标准。
- 临床试验设计与监督:对于需临床评价的二类、三类器械,瑞旭协助设计符合法规的试验方案,管理临床机构合作,并监督试验过程,确保数据真实可靠,满足注册要求。
- 上市后监管与合规维护:产品上市后,企业需履行不良事件监测、召回管理等义务。瑞旭提供定期法规更新培训、上市后研究支持,帮助企业应对NMPA的监督检查,降低违规风险。
- 国际法规协调:针对出口企业,瑞旭提供欧美、东南亚等市场的法规咨询,协助实现全球合规布局,例如CE认证、FDA注册等,提升产品国际竞争力。
三、瑞旭科技的技术咨询优势
- 专业团队:瑞旭汇聚了资深法规专家、技术工程师和临床研究员,多数成员拥有NMPA或国际机构工作背景,能精准解读政策动向。
- 本地化经验:作为扎根杭州的机构,瑞旭深谙中国监管实践,与地方药监部门保持良好沟通,可为企业提供定制化解决方案。
- 数字化工具:利用信息化平台,瑞旭为客户提供法规数据库查询、流程跟踪服务,提高咨询效率,降低人为错误。
- 案例丰富:已成功协助数百家医疗器械企业完成产品注册,涵盖影像设备、体外诊断试剂、植入材料等多个领域,口碑良好。
四、企业合作价值与未来展望
选择杭州瑞旭科技集团的咨询服务,企业不仅能节省时间和成本,更可规避合规风险,专注于产品研发与市场拓展。随着中国医疗器械法规持续演进(如人工智能器械、远程医疗产品的新规出台),瑞旭将持续更新服务内容,助力行业创新。建议企业在产品设计早期即介入法规咨询,以“合规先行”策略赢取市场先机。
医疗器械的法规合规是一项系统工程,杭州瑞旭科技集团以技术为驱动,为企业搭建了可靠的合规桥梁。无论是初创公司还是跨国企业,都能从中获得专业支持,实现在中国市场的稳健发展。